形势严峻!如何挑选顺应政策和市场潮流的品种?
密集新政爆发背后的推动因素及对行业的影响
三医联动驱动综合医改
从2009年开始,国家启动了新一轮的医改。到2014年,“新医改”基本实现了医保的全民覆盖,形成了医疗卫生治理的基本格局。
与此同时,公立医院看病难、看病贵的问题依然严重。经过多年的探索,政府意识到问题的根源在于公立医院的补偿机制是扭曲的,在过去的计划经济体制之下,医疗服务价格被严重压低和扭曲。而医疗卫生服务水平的进步依赖于资金的支持,在过去医药合业的背景下,用医药行业来补贴医疗行业的发展成了普遍现象。
医药企业通过非正常的商业贿赂、不正当的竞争等手段,来推动医药生态链的继续运转,再加上医药合业和以药补医的问题,引发了医疗机构的过度用药,“畸形”用药,引发了全行业的“医药合谋”,由此导致看病难、看病贵的问题。因此,本轮改革的焦点是医药合业、以药补医所推动的“医药合谋”,由此诞生了一个非常著名的词—“腾笼换鸟”,要把医药价值链当中药品占据的过高比重降下来,把空间留给医疗卫生服务价格,使得医务人员的劳动价值得到体现,而不必依赖于药厂的回扣。使整个医药健康的价值链趋于正常,这是本次“三医联动”改革的背后逻辑所在。
2015年2月8日国务院出台了关于完善公立医院药品集中采购的7号文,目标就是以改革公立医院的药品采购为切入点,期望最后能实现公立医院综合改革腾笼换鸟的目标,同时建立正常的补偿机制,降低虚高的药品价格,消除行业不正当竞争和商业贿赂,促进行业的整合和优化提升。
本轮改革雷厉风行,随之而来的是药品大规模的降价、压缩品规、压缩目录。然而该制度在推行过程中遇到了一定的瓶颈,希望降低药品费用、使用仿制药来替代高价原研药时,国产品的质量和疗效不足以替代价格昂贵的优质优价原研药,无法实现“腾笼换鸟”的目标,由此引发了倒逼监管行业的改革。
CFDA监管风暴
CFDA面临的压力主要有两方面:
一方面是低质的存量资产:17万个药品批文,涉及1万9千多个品种,3万9千多个品规,如此巨大的存量面临的是药监部门监管力量和监管资源的严重不足。
另一方面,医药工业也实现了逐步的转型,从低水平、重复的仿制药竞争逐步转向局部创新、跟踪仿制创新到完全创新的阶段,源源不断的增量资源在进入市场。
新增的药品注册中,受机会主义、诚信不足等行业风气的影响,存在大量的数据的真实性、完整性、可溯源性问题,行业自查由此产生,从行业的自查来制止行业增量的不良文号的进入。解决增量的问题后,国家开始重拳出击,解决存量的问题,推出了一致性评价。
自查解决增量,一致性评价解决存量,CFDA双管齐下,解决药品质量低劣的问题。
新一轮的改革思路和走向
在供给侧,药监监管理念和方式开始和国际主流接轨,建立正常态的符合药品监管客观实际需求的监管体系来强化监管,实现供给侧生产企业和药品的良性供给。
在需求侧,通过引导或医保的介入来改变医院和医生的用药行为,使整个医药价值链的分配趋于正常。
转轨的过程当中,政府的投入增长空间有限,依赖于医疗服务价格增长需要时间、需要民众的理性和科学的认识,在这个过程中,以药补医会仍然存在并延续一定的时间,但会转向更隐蔽的“明折暗扣”、二次议价等形式。
在医药合业格局下,医疗行业离不开药品的补偿,医药行业低水平重复生产/恶性竞争仍然是主旋律。由此引发医药行业价值链分配失当,相关从业人员行为扭曲,本轮改革要体现的就是三个回归,医疗、医改、医药各就其位。在以上背景下,政府对药品行业治理的逻辑可以总结为由下游需求侧倒逼所引发的“供给侧改革”。
具体表现为:强化GMP促使落后的生产企业退出;调整《药品管理法》和《药品注册分类管理办法》,通过调整围绕药品生命周期所涉及到的GLP、GSP等一系列的规范来强化行业供给者准入,提高行业整合度;通过自查核查限制不良新增的进入,通过一致性评价解决存量问题,通过调整药品注册管理办法使药品注册分类管理与国际接轨三个方面来强化药品准入,在需求侧使整个价值链的分配回归正常。
政策调整导致的行业增速放缓
2015年,新一轮招标采购的启动,残酷的二次议价带来了药品价格重心的快速下移,药品价格呈持续下行趋势并将会有1-2轮20%的降幅,带来了行业的增速放缓;
全民医保体系下,医保是卫生费用的主要付费者,医保付费已经占到了整体卫生付费的58%左右,加上由医保引发的二次消费将达到80%,医保资金穿底压力巨大,未来医保的控费将进一步强化,由此引发药品消费的进一步被压低;
国家去年出台了一系列降低药占比和采购预算,规范医生用药行为的考核方案和文件,将促进用药趋于规范;
在当前招标采购政策下,新产品的准入困难。7号文和70号文确定的医疗机构招标采购方案提出,对招标目录要以历史存量为依据,目前仅有江浙沪,广东,北京、湖北等经济发达地区允许有5%的增补,因此,新药的准入非常的困难。
招标新政影响下,对交易标的价值的再评估
药品采购新规的关键要点
药品销售市场以公立医院为主,这个市场受政府政策影响明显,根据国务院去年发布的7号文,本轮药品新政的主要关键点有:
药品采购是政府采购,受政府制定规则的制约;
分类采购。7号文提出,专利独家产品采取价格谈判策略;对于生产企业超过3家,使用金额较高的,采用双信封招标,大多数药品属于这个范畴;对于特殊的,要保证供应的,采取挂网采购,对于毒麻精放政府管制的,采取政府定价,因此交易标的属于哪种采购范畴也是要考虑的;
目录合并,目前药品供应目录是过剩的,7号文规定按照存量目录制定下轮采购目录,这一轮的治理意味着将有大量药品逐渐退出市场;
竞价分组。标的在招标中所处的质量层次决定了药品的价格层次,决定了药品价格竞争的激烈程度,决定了标的市场的未来;
区域碎片化,医保筹资以地市为筹资单元,各地招标方案不统一;
价格联动;
国产化替代、仿制药受一致性评价进程制约;
医院市场变化的溢出关系。
标的价值判断的考量点
根据以上政策,对于标的价值判断的考量点有以下几个方面:
市场属性:标的产品属于医院市场还是非医院市场,如果是医院市场就会受到国家一系列政策的直接影响。
如果在公立医院市场格局下,标的分类的采购分类属性/竞价质量层次是什么?这直接决定了标的未来的竞争态势和面临的市场环境。竞价质量层次直接决定药品价格的高低。
竞争门槛:真正的门槛取决于标的稀缺和不可替代性。
系统能力和政策相容度:系统能力包含企业政府事务能力、商务能力、招标价格谈判能力等多方面,系统能力的优胜才是真正的优胜,任何因素都有可能导致产品的掉标。在此基础上离不开标的的政策相容度,要考虑标的是政策鼓励的方向还是淘汰的方向。
采购新政下对市场的预判
2015城市等级医院公立医院总体市场规模有8000多个亿,来自于政府采购的市场总规模约13000亿左右,未来市场仍会缓步增长,7号文确定了存量目录作为采购目录,因此目前的竞争是存量市场之争。
在增量市场上,由于医保资金的限制,新品准入的通道是狭窄的。
仿制药质量一致性评价一旦有所进展,竞价层次就会被简化。多层竞价层次存在的原因就是一致性评价的滞后,使药品事实上存在不同的质量层次。
实现仿制品替代,必定是任何一个医保体系或者商保体系的必然选择。
目前不能确定的因素有:
虽然医保的政策是明朗的,但是部门之间的分歧仍然是严重的,冲突持续到何时何地并不明朗。
整个质量与疗效一致性评价的进程也不明朗,政策上虽然确定是必要的,但是整个产业并没有做好准备,整个过程可能会持续相当长一段时间,这个过程中,原研药品仍有自己的优势所在。
报销体系的不明朗。主要是由于来源于商保的因素是不确定的。
创新药价值的评估原则
整个全球医药创新近年来出现了一定程度的复苏,这是因为基础医疗的进展带来了新的治疗手段的扩展。突出的典型代表是生物药、抗体药以及转化医学带来的市场的增量等。创新药标的评估主要有以下考虑因素:
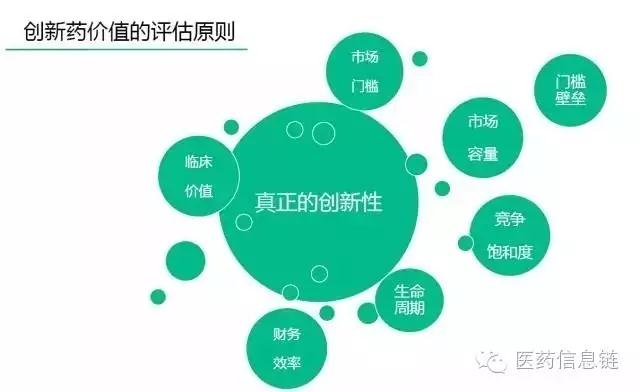
新的《药品注册管理办法》谈到了对新药的界定,提出了“全球新”和强调要满足临床上未能满足的需求。因此要关注创新程度的问题。
创新也要考虑竞争饱和度的问题,像DPP-4以及现在热门的PD-1,竞争都是非常激烈的。
仿制药标的的评估原则
价格空间:仿制药价格空间受限,在中国仿制药受价格招标采购联动的影响是非常深刻的。价格空间决定了未来的市场空间,更何况现在我们仍然不能脱离“以药补医”的基本事实。
仿制药还有一个压倒一切的问题就是一致性评价问题,这就要考虑仿制药一致性评价在这个标的中的作用是什么,标的一致性评价的成本,标的的竞争对手,或者说围绕一致性评价,有没有绿色通道,能不能走海外GMP,或者海外出口达到一定的销量等等。
几个需要直面的问题
有了以上原则,我们在面临创新药的标的时,要考虑以下问题,

在面临仿制药标的时,要考虑的问题:

对于中成药来说,虽然国家大力鼓励中医药的发展,但CFDA的审评原则,以及一些大型医院都对中药品种设置了门槛,看清到底是那种政策起主要推动作用很重要。

来源:医药信息链